氮元素也与碳元素一样存在一系列氢化物,如NH3、N2H4、N3H5、N4H6等。请回答下列有关问题:
(1)上述氮的系列氢化物的通式为____________。
(2)已知:2H2(g)+O2(g)=2H2O(g) △H=-483.6kJ·mol-1,查阅文献资料,化学键键能如下表:
化学键 | H-H | N=N | N-H |
E/kJ·mol-1 | 436 | 946 | 391 |
①氨分解反应NH3(g)
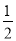 N2(g)+
N2(g)+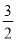 H2(g)的活化能Ea1=300kJ·mol-1,则合成氨反应
H2(g)的活化能Ea1=300kJ·mol-1,则合成氨反应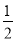
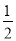 N2(g)+
N2(g)+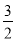 H2(g)
H2(g) NH3(g)的活化能Ea2=___________。
NH3(g)的活化能Ea2=___________。
②氨气完全燃烧生成氮气和气态水的热化学方程式为__________________________。
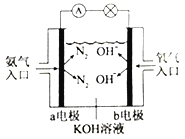
③如右图是氨气燃料电池示意图。a电极的电极反应式为________________。
(3)已知NH3·H2O为一元弱碱。N2H4·H2O为二元弱碱,在水溶液中的一级电离方程式表示为:N2H4·H2O+H2O N2H5·H2O++OH-。则可溶性盐盐酸肼(N2H6Cl2)第一步水解的离子方程式为__________________;溶液中离子浓度由大到小的排列顺序为___________________。
N2H5·H2O++OH-。则可溶性盐盐酸肼(N2H6Cl2)第一步水解的离子方程式为__________________;溶液中离子浓度由大到小的排列顺序为___________________。
(4)通过计算判定(NH4)2SO3溶液的酸碱性(写出计算过程)________________________。(已知:氨水Kb=1.8×10-5;H2SO3 Ka1=1.3×10-2Ka2=6.3×10-8)。
【答案】 NnH(n+2) 254kJ·mol-1 4NH3(g)+3O2(g)=2N2(g)+6H2O(g)△H=-1266.8kJ·mol-1 NH3+6OH--6e-=N2↑+6H2O N2H62++H2O N2H5·H2O++H+ [Cl-]>[N2H62+]>[H+]>[N2H5·H2O+]>[OH-] O32-的水解常数Kh1=
N2H5·H2O++H+ [Cl-]>[N2H62+]>[H+]>[N2H5·H2O+]>[OH-] O32-的水解常数Kh1=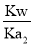 =
=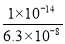 =
=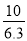 ×10-7,NH4+的水解常数Kh=
×10-7,NH4+的水解常数Kh=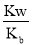 =
=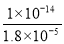 =
=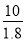 ×10-10,Kh1>Kh,故SO32-水解起主要作用而呈碱性
×10-10,Kh1>Kh,故SO32-水解起主要作用而呈碱性
(1)通过观察可知:氮与氢原子数相差2个,通式为NnH(n+2),正确答案:NnH(n+2);
(2)①NH3(g)
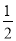 N2(g)+
N2(g)+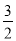 H2(g),△H=反应物的总键能-生成物的总键能=3×391-1/2×946-3/2×436=+46 kJ·mol-1; △H= Ea1- Ea2=46;300- Ea2=46,Ea2=254kJ·mol-1;
H2(g),△H=反应物的总键能-生成物的总键能=3×391-1/2×946-3/2×436=+46 kJ·mol-1; △H= Ea1- Ea2=46;300- Ea2=46,Ea2=254kJ·mol-1;
②2H2(g)+O2(g)=2H2O(g) △H=-483.6kJ·mol-1, NH3(g)
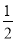 N2(g)+
N2(g)+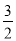 H2(g),△H==+46 kJ·mol-1;
H2(g),△H==+46 kJ·mol-1;
根据盖斯定律:两个式子整理完成后,4NH3(g)+3O2(g)=2N2(g)+6H2O(g) △H=1266.8kJ·mol-1;正确答案:4NH3(g)+3O2(g)=2N2(g)+6H2O(g) △H=1266.8kJ·mol-1;
③ 氨气燃料电池,氨气做负极,负极发生氧化反应,失去电子,在碱性环境下氧化为氮气;极反应为NH3+6OH--6e-=N2↑+6H2O;正确答案为:NH3+6OH--6e-=N2↑+6H2O;
(3)N2H4·H2O为二元弱碱,N2H6Cl2为强酸弱碱盐,水解显酸性,第一步水解的离子方程式为N2H62++H2O N2H5·H2O++H+;溶液中的离子:Cl-、N2H62+、H+、OH-、N2H5·H2O+
N2H5·H2O++H+;溶液中的离子:Cl-、N2H62+、H+、OH-、N2H5·H2O+
;根据水解规律:溶液中离子浓度大小排列顺序为:c(Cl-)>c(N2H62+)>c(H+)>c(N2H5·H2O+)
>c(OH-);正确答案:c(Cl-)>c(N2H62+)> c(H+)>c(N2H5·H2O+)>c(OH-);
(4)盐类水解平衡常数Kh=KW/Ka ,其中KW为离子积,Ka为弱酸或弱碱的电离平衡常数;
已知:氨水Kb=1.8×10-5;H2SO3 Ka1=1.3×10-2 Ka2=6.3×10-8);NH4+的水解常数Kh1=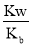 =
=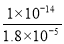 =
=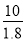 ×10-10;SO32-的水解常数Kh2=
×10-10;SO32-的水解常数Kh2=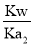 =
=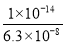 =
=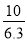 ×10-7,Kh1<Kh,平衡常数越大,水解能力就越强,故SO32-水解起主要作用而呈碱性;正确答案:碱性;已知:氨水Kb=1.8×10-5;H2SO3 Ka1=1.3×10-2 Ka2=6.3×10-8);NH4+的水解常数Kh1=
×10-7,Kh1<Kh,平衡常数越大,水解能力就越强,故SO32-水解起主要作用而呈碱性;正确答案:碱性;已知:氨水Kb=1.8×10-5;H2SO3 Ka1=1.3×10-2 Ka2=6.3×10-8);NH4+的水解常数Kh1=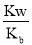 =
=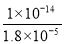 =
=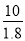 ×10-10;SO32-的水解常数Kh2=
×10-10;SO32-的水解常数Kh2=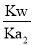 =
=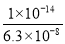 =
=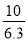 ×10-7,Kh1<Kh,平衡常数越大,水解能力就越强,故SO32-水解起主要作用而呈碱性;
×10-7,Kh1<Kh,平衡常数越大,水解能力就越强,故SO32-水解起主要作用而呈碱性;
版权声明
声明:有的资源均来自网络转载,版权归原作者所有,如有侵犯到您的权益
请联系本站我们将配合处理!
