某物质在氧气中完全燃烧,需要5.6g氧气,同时只生成4.4g二氧化碳和2.7g水,则该化合物中( )
A. 只含碳、氢两种元素
B. 只含碳、氧两种元素
C. 只含碳、氢、氧三种元素
D. 一定含碳、氢元素,可能含氧元素
【答案】A
【解析】根据质量守恒定律的实质可以知道,在反应前后元素的种类及质量不变,所以可以判断在该物质一定含有碳元素和氢元素,而二氧化碳中氧元素的质量为:
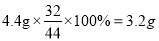 ,水中氧元素的质量为:
,水中氧元素的质量为:
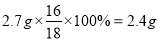 ,所以二氧化碳和水中所含氧元素的总质量为:3.2g+2.4g=5.6g,这与所消耗的氧气的质量相等,所以结合质量守恒定律的实质可以得出在该物质中不含氧元素。故选A。
,所以二氧化碳和水中所含氧元素的总质量为:3.2g+2.4g=5.6g,这与所消耗的氧气的质量相等,所以结合质量守恒定律的实质可以得出在该物质中不含氧元素。故选A。
版权声明
声明:有的资源均来自网络转载,版权归原作者所有,如有侵犯到您的权益
请联系本站我们将配合处理!
