脱去冶金工业排放烟气中SO2的方法有多种.(1)利用本生(Bunsen)热化学循环吸收SO2工艺由下列三个反应组成:2H2(g)+O2(g)═2H2O(I)△H1=-572kJ•mol-12HI(g)
问题描述:
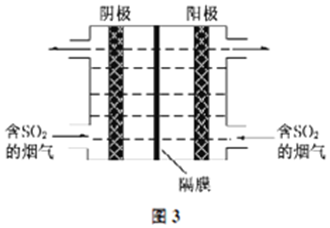
脱去冶金工业排放烟气中SO2的方法有多种.(1)利用本生(Bunsen)热化学循环吸收SO2工艺由下列三个反应组成:2H2(g)+O2(g)═2H2O(I)△H1=-572kJ•mol-12HI(g)═H2(g)+I2(g)△H2=+10kJ•mol-12H2SO4(I)═2SO2(g)+2H2O(g)+O2(g)△H3=+462kJ•mol-1则得SO2(g)+I2(g)+2H2O(I)═2HI (g)+H2SO4(I)△H=___ kJ•mol-1(2)氧化锌吸收法.配制ZnO悬浊液,在吸收塔中封闭循环脱硫.测得pH、吸收效率η随时间t的变化如图1所示;溶液中部分微粒与PH的关系如图2所示.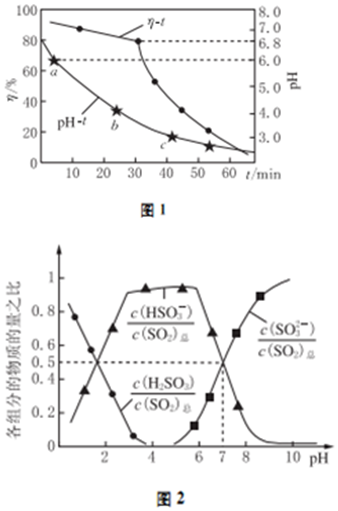 ①为提高SO2的吸收效率η,可采取的措施有:增大悬浊液中ZnO的量、___.②图1中的pH-t曲线ab段发生的主要化学方程式为___③pH=7时,溶液中
①为提高SO2的吸收效率η,可采取的措施有:增大悬浊液中ZnO的量、___.②图1中的pH-t曲线ab段发生的主要化学方程式为___③pH=7时,溶液中 | c(Zn2+) | ||
c(S
|
 最佳答案:
最佳答案: (1)①2H2(g)+O2(g)═2H2O(I)△H1=-572kJ•mol-1②2HI(g)═H2(g)+I2(g)△H2=+10kJ•mol-1③2H2SO4(I)═2SO2(g)+2H2O(g)+O2(g)△H3=+462kJ•mol-1结合盖斯定律计算,(①+2×②+③)×12得到热...
版权声明
声明:有的资源均来自网络转载,版权归原作者所有,如有侵犯到您的权益
请联系本站我们将配合处理!
