已知,在KClO3+6HCl=KCl+3Cl2↑+3H2O的反应中,若标况下产生6.72LCl2 ,
(1)用双线桥表示上述反应得失电子的情况,并指出氧化剂和还原剂
(2)计算被氧化的HCl的物质的量.
【答案】(1)
答: 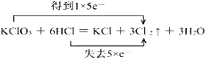 ;KClO3;HCl;
;KClO3;HCl;
(2)
答:被氧化的HCl的物质的量为0.5mol.
【解析】解:(1)该反应中,氯酸钾中氯元素的化合价由+5价变为0价,所以氯酸钾是氧化剂,HCl中Cl元素化合价由﹣1价升高到0价,被氧化,HCl是还原剂,氯气既是氧化产物也是还原产物,得电子与失电子个数相等,比值为1:1,氧化产物和还原产物的质量之比是5:1,只有Cl元素化合价发生变化,当有3mol Cl2生成时,转移5mol电子,则电子转移的方向和数目为 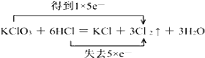 (2)反应中6molHCl中有5mol被氧化,生成3mol Cl2 , 则生成标准状况下的Cl2为6.72L即 6.72 L 22.4 m o l / L =0.3mol,被氧化的HCl为0.5mol,
(2)反应中6molHCl中有5mol被氧化,生成3mol Cl2 , 则生成标准状况下的Cl2为6.72L即 6.72 L 22.4 m o l / L =0.3mol,被氧化的HCl为0.5mol,
版权声明
声明:有的资源均来自网络转载,版权归原作者所有,如有侵犯到您的权益
请联系本站我们将配合处理!
上一篇 : 下列四种基本反应中一定属于氧化还原反应的是( )
